GCPセンター
臨床試験『治験』について
治験とは
国(厚生労働省)から新しい薬(医薬品)として承認を得るために、健康な人や患者さんの協力を得て行われる臨床試験のことを『治験』、この時に使われる『薬の候補』を『治験薬』と呼びます。
新しい薬の開発を行う場合、まず『薬の候補』になる物質を選び出し、動物において『薬の候補』 の効果と安全性を調べます。動物において効果と安全性が確認できた場合には、次に健康な人や患者さんに『薬の候補』を使用していただいて、その効果と安全性を調べます。
このように、『薬の候補』が薬として実際に患者さんに使われるようになるまでには、その『薬の候補』に病気に対して効果があるかどうか、また安全であるかどうかを確かめた上で、国から薬として承認を得る必要があります。
治験の流れ
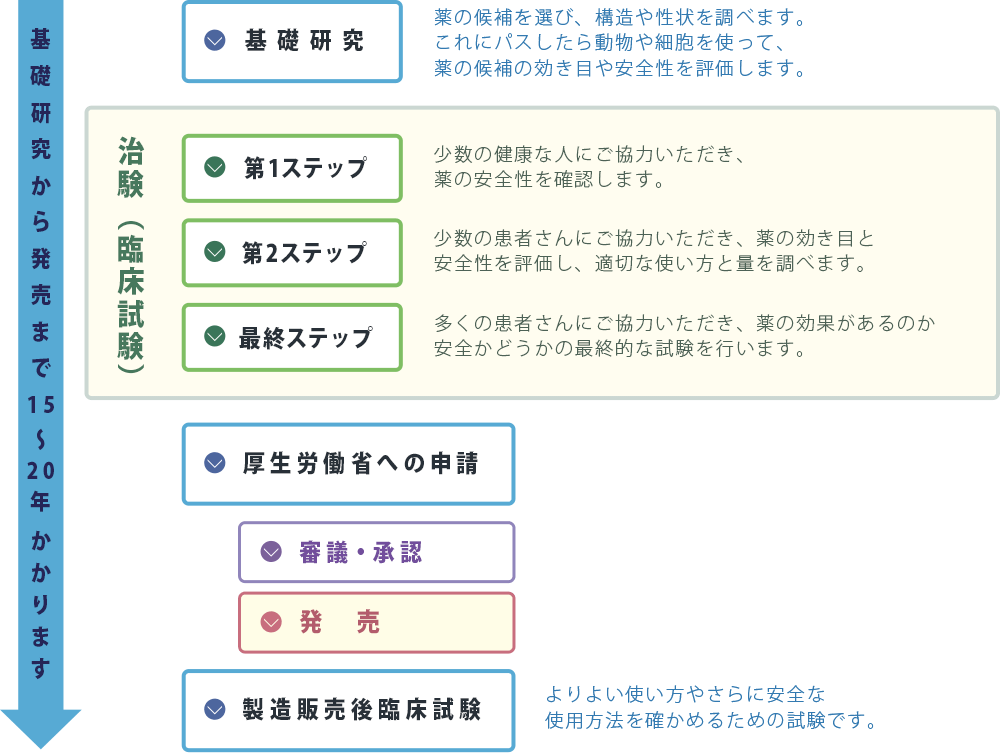
『治験』には研究的な側面がありますが、現在、あなたを含め他の多くの患者さんに使われている薬は、これまで『治験』に参加していただいた多くの方々の協力により生まれています。
治験を行う場合には、治験に参加される方々の安全と人権を守るために、国が定めた「医薬品の臨床試験の実施の基準(GCPといいます)」を遵守しなければなりません。
当院ではこのGCPに従って、科学的および倫理的な観点から、治験の実施や継続について調査・審議するため、順天堂大学医学部附属静岡病院治験審査委員会を設けています。
本治験審査委員会により内容が審議され、病院長より許可された治験のみが実施されています。





